体细胞突变是肿瘤、衰老和其他多种疾病发生发展的重要原因,建立高效准确的突变检测技术是实现健康风险监测及预警的重要途径。但是,早期突变由于基因组上发生频率极低和细胞散在发生,难以被测序错误率很高的普通二代测序技术(NGS)检测到。公共卫生学院栾洋研究员课题组自主创新建立的超低频突变检测技术有望实现任意物种体细胞上全基因组范围的突变检测,最新成果于2023年10月在Nucleic Acids Research上以题为Genome-wide direct quantification of in vivo mutagenesis using high-accuracy paired-end and complementary consensus sequencing的研究论文发表。此外,以基因突变为检测终点的人群早期效应标志也是致癌风险评估的重要工具。课题组应用人群外周血建立了PIG-A基因突变检测技术,已在致癌物职业暴露人群初步验证,近期应用于苯和多环芳烃风险评估,研究成果于同年5月和6月分别发表在Environmental Pollution和Food and Chemical Toxicology期刊。上述技术为突变研究提供了重要工具。
基于NGS的低频突变检测技术研究进展
NGS的出现为突变检测技术的革新带来契机,但是,目前普遍使用的NGS测序错误率很高(~千分之几),所以多应用于检测体细胞上发生的胚系突变、和以克隆增生为特征的肿瘤细胞或单细胞上的突变分析。而正常体细胞因环境等因素作用后全基因组上发生的微量突变负荷增加,则难以通过普通NGS检测。

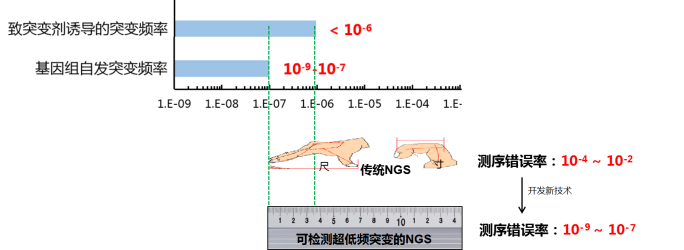
为了降低测序错误率,目前公认有效的策略是基于“分子一致性测序”的ecNGS(Error-corrected NGS)技术,简言之就是针对同一模板来源的多个拷贝测序后进行错误校正,以提高准确性。该策略最早由华盛顿大学欧洲杯竞猜平台研究者提出,命名为“Duplex Sequencing”,大大降低了测序错误率。但是因为该技术引入PCR扩增环节,目的片段产生的拷贝数过多,因此测序效率很低,迄今为止仅应用于局部的靶向测序及小型基因组;Sanger研究所基于该策略也开发了系列方法,经多次改进后,于2021年在Nature杂志上报道的“NanoSeq”技术,准确性不仅达到基因组自发突变水平,还大大提高了测序效率,并应用该技术探索了人体组织上细胞分裂程度与突变的关联。该技术代表了本领域当前国际最高水准。
原创性低频突变测序技术PECC-Seq
尽管已有上述ecNGS技术的见刊论文,但仍存在一些数据分析和技术上的壁垒使其无法被具体和广泛应用。公共卫生学院栾洋课题组经过多年研究,主导开发了自主创新的分子一致性测序方法,命名为“PECC-Seq”。技术原创点包括截短片段,PCR-free文库制备,DNA互补双链通过双端测序产生4条重叠片段,与参考基因组比对进行错误校正。该策略大大提高了NGS测序的准确性和测序效率,首篇论文于2020年在领域权威期刊Archives of Toxicology上发表后得到关注。后续又经深入分析,找到测序错误主要来源于文库制备中超声引起的单链损伤,经末端修复被固定,并应用HPLC-MS技术对损伤产物的“Artifacts”进行了确认。据此优化实验条件后,方法在准确性和测序效率上已经与“NanoSeq”技术相当。与经典的转基因动物体内突变检测技术相比,在诱变剂检测上具有更高灵敏性。该技术使得人和实验动物体细胞上全基因组范围的超低频突变检测成为可能。
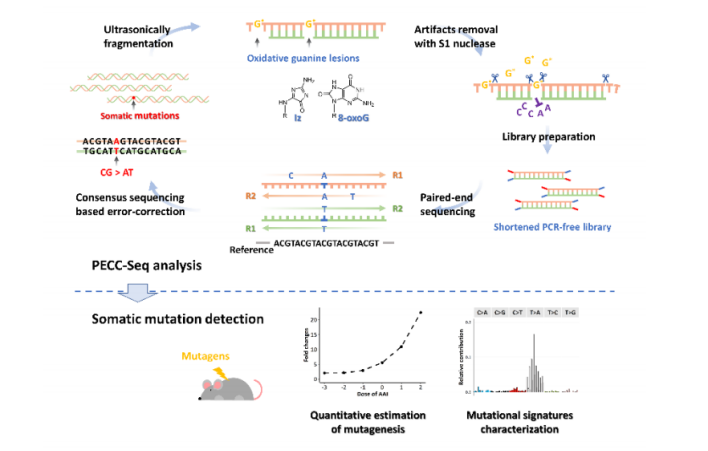
PECC-Seq技术可在任意组织检测单核苷酸突变频率,并获得突变特征,未来有望与其他毒性试验整合,替代经典体内致突变实验;除环境诱变剂外,还可用于干细胞及其衍生细胞治疗产品的安全性评价和质量控制,以及基因编辑技术中脱靶效应的评价与研究;结合DNA加合物组和暴露组分析,整合动物研究和人群研究,未来有望用于复杂环境因素与人类疾病的关联及机理研究;此外,针对已知致癌物暴露的高危人群,有望用于健康风险监测与疾病预防;最后,还可用于生命科学领域中衰老与发育研究领域,回答待解科学问题。
目前PECC-Seq技术已申请专利,研究进展在国际学术会议上多次进行报告交流并获得关注。相关论文的第一作者尤馨悦博士以该研究取得博士学位,并获得国家自然科学基金青年项目和中国博士后科学基金项目的资助。
新的遗传学损伤效应标志——人群外周血PIG-A突变检测技术
癌症发病率逐年增高,如何预警和防治外源化学诱变剂对健康的危害是重要的科学问题。因绝大多数化学致癌物具有遗传毒性,因此以检测遗传学损伤为主的毒性效应标志应用较为广泛,目前常用的技术包括检测DNA损伤的外周血彗星试验和检测染色体损伤的外周血微核试验。突变和人类肿瘤的发生密切相关,但是目前尚缺乏以检测基因突变频率为终点的人群监测方法。
细胞表面存在的许多分化抗原通过糖基磷脂酰肌醇聚糖(GPI)锚连接在细胞表面。磷脂酰肌醇聚糖A(Phosphatidylinositolglycan classA,PIG-A)基因是GPI锚的编码基因,且在与GPI锚合成相关的基因中,只有PIG-A基因位于x染色体上,因此,PIG-A基因单次突变即可导致该细胞GPI锚缺陷和表面相应抗原缺失。通过检测细胞表型(相应表面抗原是否缺失)来考察发生基因突变的细胞比例,进而计算PIG-A基因突变频率,可以评价受试物的致突变性。外周血是常用的生物学标志检测样本,骨髓造血干细胞如发生PIG-A基因突变,将导致成熟血细胞表面相应标志缺失从而被检测到。目前,在动物实验上已验证该方法有效性,2022年OECD组织将其列入法规,用于化学物临床前致突变作用的评价。
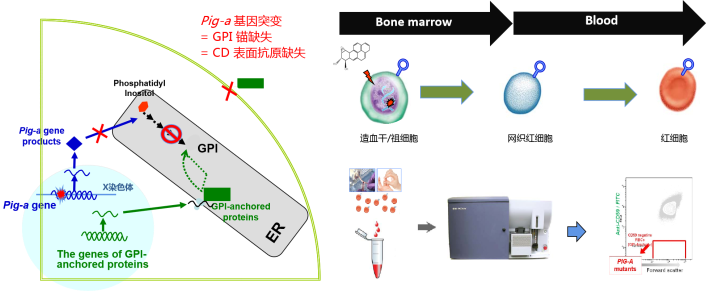
据悉,公共卫生学院栾洋研究员作为OECD专家工作组成员参与了实验动物Pig-a突变技术指南制订,课题组于2016年开始在国际上率先开展了人群研究。目前已建立检测方法,并在致癌物职业暴露人群、化疗药物治疗患者上完成了方法验证,结果表明该方法作为早期效应标志可用于致癌风险评估。目前在开展的应用研究包括苯和多环芳烃职业暴露风险研究。国际通行的苯职业暴露限值为1 ppm,主要基于造血功能障碍和白血病风险。利用人群红细胞PIG-A突变检测技术进行研究和计算,苯的安全浓度被确定为需低于0.07 ppm,该数据为监管机构修订苯的职业暴露接触限值以进行更早期风险预警提供了重要参考。上述结果于2023年5月以题为 Benchmark dose estimation for benzene-exposed workers in China: Based on quantitative and multi-endpoint genotoxicity assessments的研究论文发表在权威期刊Environmental Pollution上。此外,在焦炉工队列研究中也应用PIG-A突变检测技术对工人进行了风险监测,上述结果于2023年6月以题为PIG-A gene mutation as a mutagenicity biomarker among coke oven workers”的研究论文在Food and Chemical Toxicology上发表。综上,PIG-A基因突变频率可以成为灵敏的效应标志用于人群风险评估。需要注意的是该技术无法获得基因的突变特征,因此结合PECC-Seq和相关内暴露分析将是更好的研究策略。系列论文第一作者为公共卫生学院的曹易懿和奚晶老师。
开发新技术绝不仅仅是为了论文发表,技术只有被用起来才能获得生命力。期待未来有更多学科交叉与合作的开展,将上述技术用于化合物/生物制品和环境因素的安全性评价和人群健康风险评估,最终为监管提供理论依据,解析复杂环境暴露的毒性机理,以及回答生命科学领域中一些待解科学问题。
欧洲杯竞猜平台公共卫生学院栾洋研究员课题组研究方向为遗传毒理,主要为新技术开发和外源化合物毒性机理研究。探索的新技术包括基于一致性测序的低频突变检测方法,新遗传学损伤效应标志人外周血PIG-A基因突变试验,基于微流控和微孔板体系的单线虫高通量毒性测试方法等;此外,通过DNA加合物检测、体外培养细胞DNA损伤、染色体畸变和基因突变检测、转基因动物基因突变检测等体系,结合分子生物学手段,对环境污染物及中药有毒成分进行毒性评价和机制研究。上述研究得到国家自然科学基金项目支持(81873081,82304267,21477078,21077112,20807045)。部分研究与日本国立卫生研究院(NIHS)合作由欧洲杯竞猜平台主导完成。
课题组联系E-mail: yluan@sjtu.edu.cn