2020年5月20日,欧洲杯竞猜平台/上海市免疫学研究所王宏林研究员团队在Science Advances发表了题为“A Micropeptide Encoded by LncRNA MIR155HG Suppresses Autoimmune Inflammation via Modulating Antigen Presentation”的研究论文,报道了课题组原创性发现人基因组非编码区编码多肽miPEP155(传统观点认为非编码区基因不编码,故称“暗物质区”),miPEP155能够调控炎症环境中树突状细胞的抗原提呈能力,对小鼠类银屑病与多发性硬化症(EAE)两种自身免疫性疾病模型具有较好的治疗效果,这一多肽有望成为治疗自身免疫性疾病的创新性药物。
miRNA前体一般被认为不具备编码功能。最近的研究表明,miRNA前体及其他的长链非编码RNA含有的微小开放读码框也具有编码多肽的能力,一般小于50个氨基酸长度的肽链被称为多肽。在机体内很早就发现了一批具有生物活性的多肽,如:免疫活性肽、神经活性肽等,其潜在功能涉及人体的激素、神经、细胞生长和生殖各领域。人体内存在1881个miRNA的前体和超过20,000个长链非编码RNA。这些“非编码区”编码的多肽甚至超过了目前已知所有蛋白的种类,极大拓展了我们对于体内多肽及其功能的认识。2015年Dominique等在Nature上报道拟南芥中存在miR-165a及miR-171b前体编码多肽调控拟南芥根部的发育。但是,在哺乳动物中是否存在同样的现象仍有待于进一步的研究。
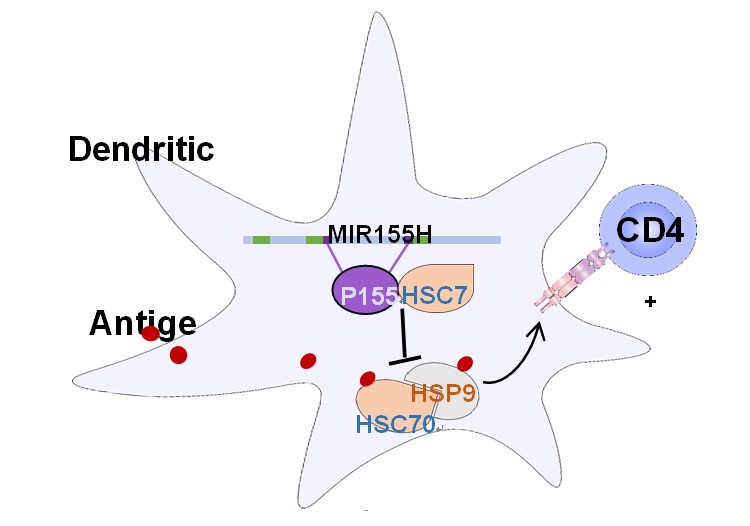
图1:miPEP155结合HCS70调控抗原提呈,治疗自身免疫性疾病
课题组运用生物信息学分析,结合数据库Ribo-seq结果,发现了人树突状细胞(Dendritic Cells,DCs)中“非编码”基因microRNA155 host gene存在编码多肽的潜能。进一步通过CRISPR技术、定制抗体等手段,首次证实了人“非编码”microRNA前体能够编码多肽,并将MIR155HG编码的这一多肽命名为miPEP155。研究人员运用Biotin标记的miPEP155发现其在DCs中的互作蛋白HSC70,并在内源性miPEP155上得到了验证。HSC70是一种分子伴侣和热休克蛋白,存在两个主要结构域,ATPase功能域与substrate-binding domain(SBD),其参与细胞内蛋白质的折叠、装配、转运和降解,维持细胞热耐受,调节细胞内突变蛋白的表达等。近年来,HSP肽复合物激活特异性免疫应答的研究得到广泛关注。体外研究发现,miPEP155可特异性地与HCS70的ATPase功能域绑定,大幅降低炎症环境中DC细胞MHC-Ⅱ的表达和转运水平,从而调控其抗原提呈功能(图 1)。
银屑病(Psoriasis)是一种常见的、高复发性皮肤免疫性炎症,临床表现为患者皮损处的角质形成细胞过度增生导致表皮增厚、结痂增多;同时真皮中有大量炎症细胞浸润。银屑病鲜有致死,但大量的皮屑常使患者瘙痒难耐、痛苦不堪,严重影响其生活品质;而且表皮结痂影响患者的外观,严重影响患者的社交及工作。在咪喹莫特诱导的小鼠类银屑病模型中,miPEP155治疗显著减少了皮肤的厚度和真皮中的炎症细胞浸润。DCs是目前发现的抗原递呈能力最强的固有免疫细胞,皮肤DCs在银屑病的发病进程中有至关重要的作用,miPEP155可能通过抑制DCs抗原提呈这一机制减轻了银屑病模型的发生发展。在另一种自身免疫性疾病小鼠模型EAE中,尾静脉注射miPEP155大幅度减缓减轻了疾病的发生发展,这为自身免疫性疾病的治疗提供了新的可能策略。
多肽具有人体内不结存,无副作用、用量少、吸收快、生产成本低廉等优点。多肽市场方面,全球多肽药物的市场已经超过200亿美元,并且保持每年10%的增速。目前全球多肽类药物的研发已广泛涉足疫苗、抗肿瘤药物、心脑血管药物、抗病毒多肽,以及抗菌性活性肽、诊断试剂盒的研究。目前全球已经批准了近60个多肽产品上市。王宏林课题组利用分子生物学及抗体检测的方法在世界范围里首次发现了miR-155前体(pri-miR-155编码多肽并命名为miR-155前体编码多肽(miPEP155)(专利申请号:201810643349.5),且在两种自身免疫性疾病的小鼠模型上明确了其生物学功能,有显著治疗效果。未来,团队有望对miPEP155结构进行进一步优化使其达到最佳的治疗效果,最终成为一种靶点明确,疗效明显,低毒副作用,成本低廉的原创性治疗自身免疫性疾病的多肽类药物。
王宏林,上海市免疫学研究所研究员,欧洲杯竞猜平台特聘教授,博士生导师,国家杰出青年基金获得者,长期从事银屑病研究,在银屑病病因学和治疗新靶点领域取得了系列原创性研究成果。该研究由王宏林团队独立攻克,成果具有较强的临床转化潜力,王宏林团队在新药研发领域一直成果突出,具有成功获得国家I类新药临床批件的经验与实力。上海市免疫学研究所王宏林研究员为该论文的通讯作者,博士后牛立慢、楼方舟、助理研究员孙洋为该论文的共同第一作者。该研究受到国家杰出青年科学基金、国家自然科学基金面上及青年项目、上海市转化医学协同创新中心项目及上海市高水平地方高校创新研究团队计划的支持。该研究得到上海市免疫学研究所,包括免疫所的流式平台,显微成像平台,测序平台等公共平台的支持。
作者:牛立慢,楼方舟,孙洋
编辑:王佳琦,冯昫皎
审核:方丽娟,李斌
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@sjtu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@sjtu.edu.cn