Cell Metabolism | 上海市免疫学研究所邹强课题组、叶幼琼课题组及合作团队揭示膳食果糖增强肿瘤免疫应答的机制
发布日期:2023-10-20
2023年10月19日,欧洲杯竞猜平台上海市免疫学研究所邹强研究团队等在Cell Metabolism杂志在线发表了题为“Dietary fructose-mediated adipocyte metabolism drives antitumor CD8+ T cell responses”的研究论文。该研究揭示了一条免疫内分泌通路:果糖-脂肪细胞-瘦素- CD8+ T细胞轴,描述了膳食果糖在塑造脂肪细胞代谢以启动抗肿瘤CD8+ T细胞反应中的关键作用,提示该免疫内分泌通路潜在的癌症免疫治疗方案可能性。
摄入糖类能促进人体大脑中的多巴胺分泌,故而摄入糖类含量高的食物能使人感到更快乐[1]。近年来,果葡糖浆、高果糖玉米糖浆类调味剂的使用量大大增加。果糖是葡萄糖的一种同分异构体,个人日常所摄入果糖总量的40~60%来源于水果、蜂蜜以及蔗糖;另一主要来源是由淀粉水解为葡萄糖后,葡萄糖通过多元醇途径转化为果糖。
多项研究发现,过量摄入果糖与肥胖、糖尿病和脂肪肝等代谢性疾病密切相关[2]。近日,国内研究团队证实了高果糖在小鼠模型中能促进肝癌进展[3]以及在小鼠模型中果糖代谢可促进肠道肿瘤发生肝转移[4],揭示了果糖对于肿瘤细胞生长的促进作用,但是果糖对肿瘤微环境中分子、代谢及免疫特性的影响仍有待确定。在本研究中,研究团队通过构建高果糖饲喂小鼠模型并接种皮下肿瘤发现,果糖饲喂组小鼠肿瘤生长更缓慢,且小鼠生存时间显著延长。这与之前广泛认为的“果糖促癌”的观点相反,果糖甚至可以抑制小鼠皮下肿瘤生长。
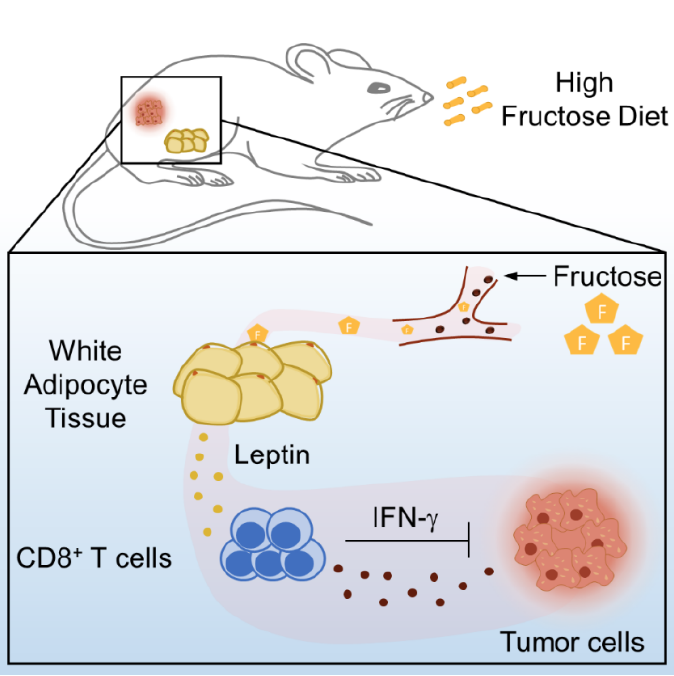
结合单细胞测序、多种敲除鼠模型以及大数据分析,研究团队发现,高果糖饮食抑制小鼠皮下瘤生长主要机制是CD8+ T细胞在其中发挥了关键作用。研究结果显示,在果糖饲喂条件下,小鼠肿瘤微环境中的CD8+ T细胞耗竭减少,增殖更多且细胞因子IFNy分泌增多。在特异性敲除T细胞果糖转运蛋白GLUT5后,果糖饲喂组小鼠依然展现出更缓慢的肿瘤生长速度以及更强劲的CD8+ T细胞抗肿瘤能力。进一步通过蛋白芯片对血清中炎症相关蛋白进行分析发现,果糖通过诱导脂肪细胞中mTORC1依赖性瘦素的产生,增加了小鼠血清和肿瘤微环境中瘦素的水平。研究团队进一步从肺癌患者肿瘤样本和血液样本中分析发现,肺癌患者血浆中果糖浓度与瘦素水平呈正相关,且血浆中瘦素水平和肿瘤微环境内抗肿瘤CD8+ T细胞功能提升相关。以上研究阐明了一条免疫内分泌通路:果糖-脂肪细胞-瘦素- CD8+ T细胞轴,揭示了膳食果糖在塑造脂肪细胞代谢以启动抗肿瘤CD8+ T细胞反应中的关键作用,提示该免疫内分泌通路作为潜在的癌症免疫治疗方案可能性。
欧洲杯竞猜平台上海市免疫学研究所博士生张月榕、副研究员于晓彦和技术员包汝娟为文章的共同一作。欧洲杯竞猜平台上海市免疫学研究所邹强研究员、欧洲杯竞猜平台附属上海市胸科医院孙加源主任、欧洲杯竞猜平台附属瑞金医院赵任主任和欧洲杯竞猜平台上海市免疫学研究所叶幼琼研究员为文章的通讯作者。

邹强研究员,国家杰出青年人才,现任欧洲杯竞猜平台基础欧洲杯竞猜平台副院长、肿瘤系统医学全国重点实验室副主任、中国生物物理学会自由基生物学与自由基医学分会理事、中国抗癌协会肿瘤微环境专委会青年委员。2016年就职于欧洲杯竞猜平台上海市免疫学研究所,长期致力于肿瘤免疫的代谢调控机制研究,探索干预肿瘤免疫代谢提高肿瘤免疫应答的免疫治疗策略,已经取得了一系列重要学术成果,以通讯作者在Cell Metabolism、Molecular Cell、Journal of Clinical Investigation、Journal of Experimental Medicine等学术期刊发表多篇论文。主持国家自然科学基金杰出青年项目、优秀青年项目、重点项目、面上项目等,2023年获得上海市卫生健康系统第十九届“银蛇奖”二等奖。
1. Edwin Thanarajah, S., et al., Habitual daily intake of a sweet and fatty snack modulates reward processing in humans. Cell Metab, 2023. 35(4): p. 571-584 e6.
2. Febbraio, M.A. and M. Karin, "Sweet death": Fructose as a metabolic toxin that targets the gut-liver axis. Cell Metab, 2021. 33(12): p. 2316-2328.
3. Zhou, P., et al., High dietary fructose promotes hepatocellular carcinoma progression by enhancing O-GlcNAcylation via microbiota-derived acetate. Cell Metab, 2023.
4. Bu, P., et al., Aldolase B-Mediated Fructose Metabolism Drives Metabolic Reprogramming of Colon Cancer Liver Metastasis. Cell Metab, 2018. 27(6): p. 1249-1262 e4.
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@sjtu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@sjtu.edu.cn