朱莉莉 青年研究员
邮箱: lili.zhu@shsmu.edu.cn
研究方向: 干细胞-类器官系统;视网膜疾病机制与治疗策略研究
教育经历
2006-2012 中国科学院上海生命科学研究院,干细胞与发育生物学博士
2002-2006 山东大学,生物科学学士
工作经历
2022.11-至今 欧洲杯竞猜平台松江研究院,课题组长/青年研究员
2017-2022 美国格莱德斯通研究所(Gladstone Institutes)/UCSF,博士后/科学家
2012-2017 英国纽卡斯尔大学,研究助理(Research Associate)
朱莉莉,课题组长,国家海外人才引进项目,上海市青年领军人才(海外)。山东大学生物学学士,中国科学院健康科学研究所干细胞与发育生物学博士,英国纽卡斯尔大学和加州大学旧金山分校/格莱德斯通研究所(Gladstone Institutes)任博士后/研究科学家。2022年11月加入欧洲杯竞猜平台松江研究院任课题组长,主要以多能干细胞和类器官为工具研究视网膜的发育与疾病。研究成果以第一作者(含并列)发表在Cell Stem Cell, Circulation, Nature Communications, JCB, EMBO Reports等国际重要学术刊物上,于2020年获得国际干细胞协会颁发的的Award for Scientific Excellence等奖项。
实验室链接:https://www.x-mol.com/groups/zhu_lab
 朱莉莉 青年研究员
朱莉莉 青年研究员
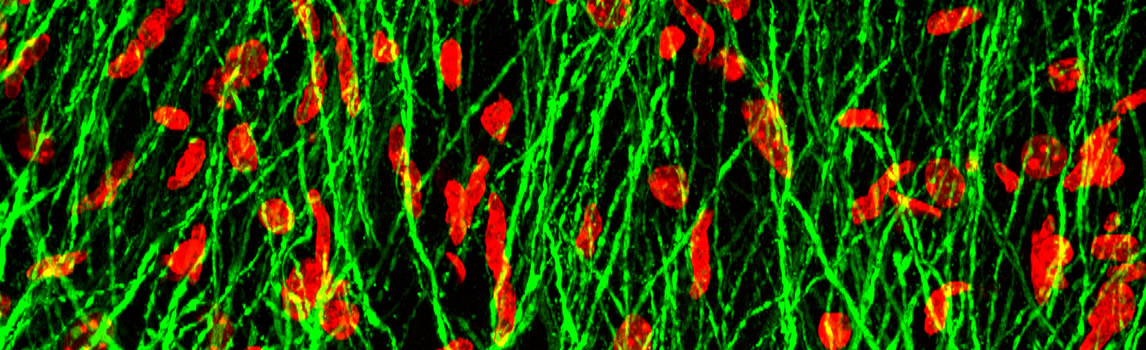
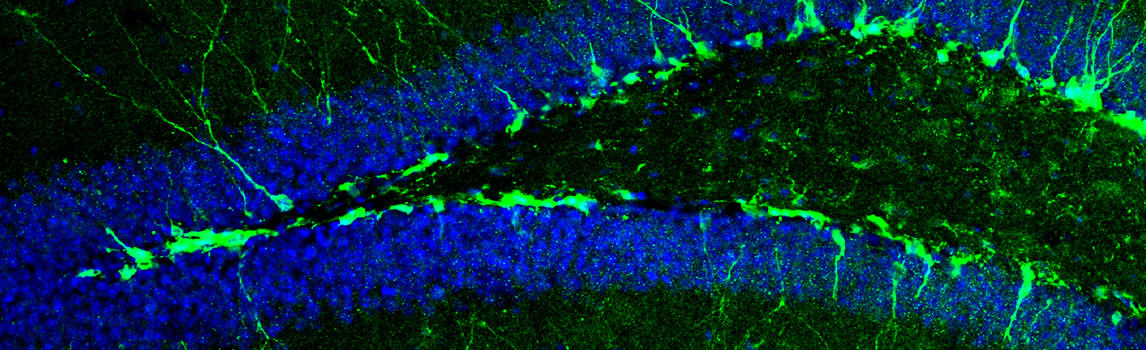
实验室的主要研究兴趣为多能干细胞,类器官和视网膜疾病的发病机制与治疗策略视力障碍及失明是当前危害全球人类健康生活的重要问题之一。最常见的造成不可逆的视力失明的原因之一即视网膜退行性病变。对视网膜退行性疾病的发病机制与治疗策略的研究具有重要意义。课题组以人多能干细胞为工具围绕视网膜疾病的发病机制以及探索潜在的治疗策略开展研究。我们将结合多能干细胞,类器官分化,分子生物学,动物模型等技术手段将完善视网膜研究的模型,揭示视网膜疾病的病理机制,探索视网膜退行性疾病的有效的临床治疗手段。未来课题组拟开展:(A)建立和完善人多能干细胞的3D视网膜类器官的分化体系;(B)利用患者来源的人的多能干细胞模拟视网膜疾病;(C)探索以干细胞为基础的治疗神经致盲眼病的临床转化
-
Zhang Z#, Li C#, Li Q, Su X, Li J, Zhu L, Lin XJ, Shen J*(2023). Structure prediction of novel isoforms from uveal melanoma by AlphaFold. Sci Data10(1):513.

-
Zhu L, Choudhary K, Gonzalez-Teran B, Ang Y, Thomas R, Bruneau B, Steinmetz L, Krogan N, Pollard K, Srivastava D* (2022). Transcription factor GATA4 regulates cell type–specific splicing through direct interaction with RNA in human induced pluripotent stem cell–derived cardiac progenitors. Circulation 146:770-787.

-
Buskin A#, Zhu L# Chichagova V, Basu B, Mozaffari-Jovin S, Grellscheid SN, Johnson CA, Lako M* (2018). Disrupted alternative splicing for genes implicated in splicing and ciliogenesis causes PRPF31 retinitis pigmentosa. Nat Commun 9:4234.

-
Zhu L, Gomez-Duran A, Saretzki G, Jin S, Tilgner K, Melguizo-Sanchis D, Anyfantis G, Al-Aama J, Vallier L, Chinnery P, Lako M, Armstrong L* (2016). The mitochondrial protein CHCHD2 primes the differentiation potential of human induced pluripotent stem cells to neuroectodermal lineages. J Cell Biol 215:187-202.

-
Zhu L#, Zhang S#, Jin Y* (2014). Foxd3 counteracts NFAT-induced differentiation to maintain self-renewal of embryonic stem cells. EMBO Rep 15:1286-96.

-
Li X#, Zhu L#, Yang A, Lin J, Tang F, Jin S, Wei Z, Li J, Jin Y* (2011). Calcineurin-NFAT signalling critically regulates early lineage commitment in mouse embryonic stem cells and embryos. Cell Stem Cell 8:46-58.









 当前位置:
当前位置:



